| |
| |  |
W najwiΩkszym skr≤cie, zaka┐enie HIV wywo│uje dysregulacjΩ odpowiedzi odporno£ciowej, a┐ do ca│kowitego jej zniszczenia. Bezpo£rednie skutki zaka┐enia - daj╣ w rezultacie zaburzenia odporno£ciowe. Te z kolei s╣ po£rednim pod│o┐em zaka┐e± drobnoustrojami oportunistycznymi i rozwoju nowotwor≤w. Pomimo olbrzymich postΩp≤w wiedzy na ten temat patogenezy zaka┐enia HIV, nie jest ona jeszcze w pe│ni poznana. Utrudnieniem jest tu brak odpowiedniego modelu do£wiadczalnego na zwierzΩtach. Poni┐ej zostan╣ przedstawione podstawowe informacje z tego zakresu. HIV to de facto heterogenna grupa wirus≤w, zaka┐aj╣cych ustr≤j poprzez wolne cz╣stki lub zainfekowane kom≤rki. Dotyczy to zar≤wno kom≤rek kr╣┐╣cych w krwi, jak i zlokalizowanych w b│onie £luzowej(szyjka macicy, cewka moczowa). Poza tym, przej£cie wirusa mo┐e odbywaµ siΩ z zaka┐onej kom≤rki do kom≤rek wchodz╣cych w sk│ad utkania b│ony £luzowej (jelito, jama macicy). Zaka┐enie r≤┐nych kom≤rek mo┐liwe jest tak┐e przez inne receptory ani┐eli CD4. Wra┐liwe na nie s╣ wiΩc kom≤rki posiadaj╣ce cechΩ fenotypow╣ CD4+ oraz jej nie posiadaj╣ce (CD4-). Do pierwszych nale┐╣: limfocyty CD4, monocyty/makrofagi (kr╣┐╣ce monocyty, pΩcherzyk≤w p│ucnych, m≤zgowe - mikroglej). Do drugich za£: kom≤rki £r≤db│onkowe, nab│onkowe, astroglej, oligodendroglej, kom≤rki Langerhansa sk≤ry (tzw. paj╣kowate jasne), dendrytyczne wΩz│≤w ch│onnych i prawdopodobnie tak┐e inne. Z monocytami wirus jest roznoszony po ca│ym ustroju, poniewa┐ z tej puli kom≤rkowej wywodz╣ siΩ makrofagi tkankowe. Pierwotne zaka┐enie HIV przebiega u 30-60% os≤b z objawami klinicznymi, najczΩ£ciej o charakterze nieswoistym, rzadziej zespo│u mononukleozowego, jeszcze rzadziej - limfocytarnego zapalenia opon m≤zgowo-rdzeniowych, a wyj╣tkowo z powa┐niejszymi (£pi╣czka) cechami zajΩcia m≤zgu. Okres ten charakteryzuje siΩ wysokimi warto£ciami wiremii oraz zaka┐eniem licznych mononuklear≤w krwi obwodowej. Jednocze£nie w surowicy wystΩpuje antygen p24. Liczba limfocyt≤w CD4 jest obni┐ona. W£r≤d subpopulacji limfocyt≤w CD4 zmniejszeniu ulega liczba limfocyt≤w o fenotypie CD4+CD45RA+ (limfocyty dziewicze) i CD45RO+ (limfocyty pamiΩci). Po kr≤tkotrwa│ym spadku, zwiΩksza siΩ liczba limfocyt≤w CD8 wykazuj╣cych cechy pobudzenia. Wskaƒnik CD4:CD8 jest odwr≤cony. ZwiΩksza siΩ tak┐e, do warto£ci zbli┐onych do zwyk│ych, liczba limfocyt≤w CD4, lecz nie ulega odbudowie subpopulacja kom≤rek pamiΩci. We wczesnych okresach zaka┐enia stwierdza siΩ zar≤wno liczne cz╣stki wirusa, jak r≤wnie┐ kopie genomowego RNA w surowicy krwi. Poni┐szy schemat jest zestawieniem etap≤w pierwotnego zaka┐enia HIV. WnikniΩcie wirusa -> Depozyt w wΩz│ach ch│onnych -> Prezentacja antygen≤w limfocytom B i T -> Aktywacja kom≤rek CD4+T -> Zaka┐enie, integracja genomu -> Rozsiew wirusa -> Cytotoksyczna odpowiedƒ kom≤rek CD4+T Po okresie zaka┐enia ostrego i pojawieniu siΩ anty-HIV dochodzi do okresu zaka┐enia bezobjawowego. Wynosi on £rednio oko│o 10 lat, z przedzia│em zmienno£ci od 7,9 do 12,3 lat. Brak replikacji nazywamy stanem zaka┐enia utajonego, a stan replikacji - zaka┐eniem produktywnym. Zaka┐enie utajone mo┐e trwaµ przez ca│e lata. w tym okresie stwierdza siΩ liczne cz╣stki wirusa, przede wszystkim w kom≤rkach dendrytycznych wΩz│≤w ch│onnych. W wielu badaniach wykazano, ┐e w okresie utajenia we krwi i w kom≤rkach znajduje siΩ mniej zar≤wno cz╣stek HIV, jak i HIV-1 RNA ani┐eli w krwi chorych z pe│ni rozwiniΩtym AIDS. We frakcji kom≤rkowej p│yn≤w ustrojowych znajduje siΩ 50-100 wiΩcej zaka┐onych kom≤rek ani┐eli wynosi liczba wolnych cz╣stek HIV. Stan zaka┐enia bezobjawowego, trwaj╣cy ca│e lata, jest mo┐liwy dziΩki - do czasu sprawnej - kontroli nad procesami replikacji HIV, sprawowanej przez uk│ad odporno£ciowy. Bez tej aktywno£ci populacja wirusa ulega│aby podwojeniu £rednio raz na dwa dni (codziennie powstaje co najmniej miliard nowych cz╣steczek wirusowych). / Poradnik dla stomatolog≤w /
| |  |
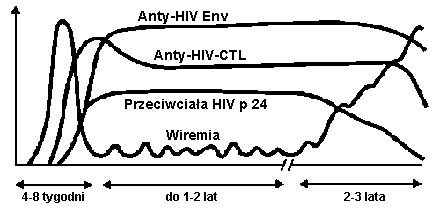
Pocz╣tkowo w surowicy stwierdza siΩ przeciwcia│a klasy IgM swoiste dla epitop≤w bia│ek p24 i gp41, a nastΩpnie przeciwko innym antygenom. Po up│ywie kilku tygodni w surowicy s╣ obecne anty-HIV klasy IgG. Szczeg≤ln╣ uwagΩ, z punktu widzenia mechanizm≤w patogenetycznych, zwraca siΩ na w│a£ciwo£ci przeciwcia│ anty-HIV typu neutralizuj╣cego (hamuj╣ce zaka┐enie kom≤rek). Wykrywa siΩ je w surowicy, p│ynie m≤zgowo-rdzeniowym i moczu. Podstawowymi determinantami indukuj╣cymi ich powstawanie s╣ epitopy umiejscowione w regionie gp120 i gp 41. S╣ to przeciwcia│a niejednorodne, skierowane zar≤wno przeciwko strukturom zmiennym, jak i konserwatywnym. Oddzia│uj╣ wiΩc zar≤wno swoi£cie dla danego typu wirusa, jak i maj╣ w│a£ciwo£ci grupowo-specyficzne. Jednak┐e ich skuteczno£µ neutralizacyjna jest ma│a. Przyczyn╣ mo┐e byµ niskie miano. Doniesiono tak┐e o nasilaniu zaka┐enia kom≤rek przez umo┐liwienie wychwytywania kompleksu wirus - przeciwcia│o, wi╣┐╣cego siΩ przez fragment Fc z receptorem kom≤rki docelowej. Poza tym przeciwcia│a anty-HIV (anty-gpl20 i anty-gp41, klasy IgG1) bior╣ udzia│ w cytotoksyczno£ci kom≤rkowej zale┐nej od przeciwcia│ (ADCC: antibody-dependent cellular cytotoxicity). Liza zaka┐onej kom≤rki nimi op│aszczonej, odbywa siΩ bez udzia│u dope│niacza. Nie ma korelacji pomiΩdzy obecno£ci╣ tych przeciwcia│ a stanem klinicznym. / Poradnik dla stomatolog≤w /
| |  | Na zr≤┐nicowanie w│a£ciwo£ci HIV maj╣ zar≤wno biologiczne cechy szczepu, jak i oddzia│ywanie £rodowiska ustrojowego. Jest to proces dynamiczny. Wszystkie izolaty uzyskane od os≤b £wie┐o zaka┐onych maj╣ przede wszystkim tropizm do makrofag≤w, co wskazuje na te kom≤rki jako na pierwsze, w kt≤rych dosz│o do replikacji bezpo£rednio po infekcji. Z czasem jej trwania tropizm wyraƒnie zmienia siΩ w kierunku limfocyt≤w CD4. Z punktu widzenia biologicznego wirusy HIV mo┐na podzieliµ na trzy grupy: izolaty o ma│ej zdolno£ci replikacyjnej i bez zdolno£ci do tworzenia zesp≤lni (NSI, non-syncytium inducing), o wysokiej replikatywno£ci, r≤wnie┐ nie tworz╣ce zesp≤lni oraz wysoko replikacyjne, tworz╣ce zesp≤lnie (SI, syncytium inducing). Izolaty SI maj╣ tendencjΩ do szybszego namna┐ania siΩ, NSI natomiast mog╣ replikowaµ siΩ zar≤wno szybciej, jak i wolniej. Tropizm do makrofag≤w jest charakterystyczny dla fenotypu NSI, jednak┐e kom≤rki te ulegaj╣ tak┐e zaka┐eniu przez HIV o fenotypie SI. Zaka┐enia wirusem SI s╣ jednak rzadkie w okresie trwania obecnej epidemii. Fenotyp SI jest zwi╣zany z tropizmem do kom≤rek T, powoduje szybsze zmniejszanie siΩ liczby kom≤rek CD4 i szybszy postΩp zaka┐enia. Wariant ten jest wykrywany u 50% chorych wykazuj╣cych progresjΩ do AIDS. Poniewa┐ po rozwiniΩciu siΩ AIDS nadal utrzymuje siΩ tendencja do dominacji wirusa o fenotypie SI, mo┐liwe jest, i┐ zmiana tropizmu z makrofag≤w do kom≤rek T jest o odzwierciedleniem osi╣gniΩcia ko±cowego etapu czynno£ciowego niedoboru odporno£ciowego. Prawdopodobnie pod wp│ywem presji immunologicznej odmiana wirusa o ma│ej cytopatyczno£ci z czasem wykazuje jej wzrost. / Poradnik dla stomatolog≤w /
| |  |
Na zr≤┐nicowanie w│a£ciwo£ci HIV maj╣ zar≤wno biologiczne cechy szczepu, jak i oddzia│ywanie £rodowiska ustrojowego. Jest to proces dynamiczny. Wszystkie izolaty uzyskane od os≤b £wie┐o zaka┐onych maj╣ przede wszystkim tropizm do makrofagow, co wskazuje na te kom≤rki jako na pierwsze, w kt≤rych dosz│o do replikacji bezpo£rednio po infekcji. Z czasem jej trwania tropizm wyraƒnie zmienia siΩ w kierunku limfocyt≤w CD4. Z punktu widzenia biologicznego wirusy HIV mo┐na podzieliµ na trzy grupy: izolaty o ma│ej zdolno£ci replikacyjnej i bez zdolno£ci do tworzenia zesp≤lni (NSI, non-syncytium inducing), o wysokiej replikatywno£ci, r≤wnie┐ nie tworz╣ce zesp≤lni oraz wysoko replikacyjne, tworz╣ce zesp≤lnie (SI, syncytium inducing). Izolaty SI maj╣ tendencjΩ do szybszego namna┐ania siΩ, NSI natomiast mog╣ replikowaµ siΩ zar≤wno szybciej, jak i wolniej. Tropizm do makrofag≤w jest charakterystyczny dla fenotypu NSI, jednak┐e kom≤rki te ulegaj╣ tak┐e zaka┐eniu przez HIV o fenotypie SI. Zaka┐enia wirusem SI s╣ jednak rzadkie w okresie trwania obecnej epidemii. Fenotyp SI jest zwi╣zany z tropizmem do kom≤rek T, powoduje szybsze zmniejszanie siΩ liczby kom≤rek CD4 i szybszy postΩp zaka┐enia. Wariant ten jest wykrywany u 50% chorych wykazuj╣cych progresjΩ do AIDS. Poniewa┐ po rozwiniΩciu siΩ AIDS nadal utrzymuje siΩ tendencja do dominacji wirusa o fenotypie SI, mo┐liwe jest, i┐ zmiana tropizmu z makrofag≤w do komorek T jest o odzwierciedleniem osi╣gniΩcia ko±cowego etapu czynno£ciowego niedoboru odporno£ciowego. Prawdopodobnie pod wp│ywem presji immunologicznej odmiana wirusa o ma│ej cytopatyczno£ci z czasem wykazuje jej wzrost. / Poradnik dla stomatolog≤w /
| |  |
W zaka┐eniu HIV - efekt immunosupresji jest zwi╣zany z zaburzeniami czynno£ci tych kom≤rek i z zmniejszeniem siΩ ich liczebno£ci. CzΩ£µ zaka┐onych limfocyt≤w CD4 ulega efektowi cytopatycznemu, a czΩ£µ - zaka┐eniu utajonemu. Odsetek zaka┐onych limfocyt≤w CD4 siΩga kilkudziesiΩciu procent, £rednio dziesiΩciokrotnie wiΩcej, ani┐eli wskazywa│y na to wyniki bada± z po│owy lat 80., uzyskane przy u┐yciu mniej czu│ych metod. Osoby zaka┐one, wg jednej z serii bada±, trac╣ rocznie - £rednio 60 x 106 / L CD4. Utrata tak znacznej liczby tych kom≤rek jest m.in. zwi╣zana z pojawianiem siΩ szczep≤w o zwiΩkszonej wirulencji. Gin╣ kom≤rki pojedyncze oraz ich zespo│y. îmierµ kom≤rki pojedynczej jest prawdopodobnie zwi╣zana z nagromadzeniem siΩ niezintegrowanego DNA wirusowego (zahamowanie syntezy w│asnych bia│ek). Kom≤rki zaka┐one HIV, wykazuj╣ce tylko ekspresjΩ bia│ek otoczki gp 120 i gp 160, a tak┐e nie zaka┐one, mog╣ tworzyµ zesp≤lnie. S╣ to twory wielokom≤rkowe po│╣czone b│onami kom≤rkowymi poprzez mostki: receptor CD4-bia│ko otoczki. Rzadko wystΩpuj╣ in vivo. Kom≤rki zesp≤lni nie mog╣ wype│niaµ swego programu genetycznego. Szybko gin╣. Rozwa┐any jest tak┐e mechanizm £mierci limfocyt≤w CD4 (lecz tak┐e CD8) poprzez tzw. programowan╣ £mierµ kom≤rki (apoptosis). W│a£ciwo£ci wzbudzania apoptozy w s╣siednich kom≤rkach ma posiadaµ kompleks gp120+receptor CD4. Inn╣ mo┐liwo£ci╣ wywo│ywania tego efektu mo┐e byµ zdolno£µ HIV do modyfikowania funkcji takich kom≤rek, jak monocyty i kom≤rki dendrytyczne. Mia│yby one utraciµ zdolno£µ do blokowania sygna│≤w o w│a£ciwo£ciach uruchamiania apoptozy w kom≤rkach T. Byµ mo┐e oddzia│uj╣ w tym procesie tak┐e superantygeny pochodzenia drobnoustrojowego lub kodowane przez wirus HIV. Superantygen ma w│a£ciwo£ci aktywowania licznych klon≤w limfocyt≤w T w spos≤b prowadz╣cy do apoptozy. Apoptoza prawdopodobnie zachodzi przede wszystkim w narz╣dach limfatycznych, w miejscu ┐ywej odpowiedzi odporno£ciowej, tam gdzie gromadzi siΩ najwiΩcej materia│u wirusowego. Doprowadza to do niedoboru dojrza│ych limfocyt≤w T. Natomiast apoptoza w grasicy i w szpiku kostnym powoduje niedostatek kom≤rek progenitorowych z konsekwencjami dla mo┐liwo£ci uzupe│nienia braku kom≤rek dojrza│ych. PostΩpuj╣cy ubytek kom≤rek dendrytycznych w wΩz│ach ch│onnych i nab│onkowych w grasicy, co obserwuje siΩ w zaawansowanych okresach zaka┐enia, mo┐e byµ przyczyn╣ braku oddzia│ywania odpowiednich sygna│≤w hamuj╣cych procesy programowanej £mierci kom≤rki. Jest to jeden z element≤w chaosu informacyjnego, kt≤ry ostatecznie wprowadza HIV w ustroju. Dysfunkcja limfocyt≤w CD4 nie zale┐y wy│╣cznie od ich niedoboru ilo£ciowego, lecz tak┐e od wi╣zania siΩ gp120 z cz╣stk╣ CD4. Zaburza to odbi≤r i przep│yw informacji do kom≤rki i z kom≤rki. Limfocyt CD4 traci zdolno£µ do rozpoznawania drobnoustrojowych antygen≤w rozpuszczalnych. Limfocyty CD4 z przy│╣czon╣ do powierzchni b│ony kom≤rkowej cz╣stk╣ CD4 mog╣ byµ tak┐e podatne na atak immunologiczny ze strony limfocyt≤w T cytotoksycznych. Przeciwcia│a przeciwko gp120 HIV mog╣ tak┐e indukowaµ przeciwcia│a antyidiotypowe imituj╣ce strukturalnie epitopy gp120. DziΩki temu s╣ one wi╣zane z powierzchni╣ b│ony kom≤rkowej limfocytu poprzez cz╣steczkΩ CD4. Tak zmienione limfocyty mog╣ byc rozpoznawane jako obce i ulegaµ niszcz╣cemu atakowi kom≤rek K - w mechanizmie cytotoksyczno£ci kom≤rkowej zale┐nej od przeciwcia│ (ADCC).
Do £mierci limfocyt≤w o fenotypie CD4 mog╣ przyczyniaµ siΩ tak┐e procesy o pod│o┐u autoimmunologicznym. PomiΩdzy cz╣steczkami HLA klasy II a gp120 i gp 40 HIV wystΩpuj╣ analogie strukturalne. Tak wiΩc, anty-HIV mog╣ reagowaµ krzy┐owo z antygenami HLA-II. W ten spos≤b blokuj╣ interakcjΩ pomiΩdzy limfocytami CD4 a cz╣steczkami HLA-II na kom≤rkach prezentuj╣cych antygen. Uniemo┐liwia to w│asciw╣ odpowiedƒ na antygeny. Zaburzenia te pojawiaj╣ siΩ jeszcze przed zmniejszeniem siΩ liczby tych kom≤rek. Poni┐sza rycina przedstawia schematyczny przebieg zaka┐enia HIV-1, uwzglΩdniaj╣cy takie elementy, jak poziom wiremii, liczbΩ limfocyt≤w CD4 etc.
Ryc. Schemat przebiegu zaka┐enia HIV-1 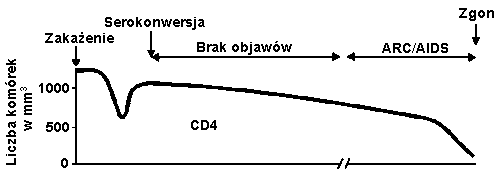
/ Poradnik dla stomatolog≤w /
| |  |
Zaka┐enie omawianym tu wirusem powoduje uruchomienie odporno£ciowych mechanizm≤w obronnych. Badania przeprowadzone w po│owie lat 90. wykaza│y, i┐ replikacja HIV utrzymuje siΩ na do£µ wysokim poziomie podczas okresu bezobjawowego. Niszczeniu ulegaj╣ liczne kom≤rki uk│adu odporno£ciowego. Mimo to, na skutek funkcjonowania mechanizm≤w obronnych, do za│amania siΩ odporno£ci dochodzi dopiero po latach. Przez £rednio 10 lat poziom wirusa stopniowo wzrasta, czemu towarzyszy zmniejszanie siΩ liczby limfocyt≤w pomocniczych o fenotypie CD4. Przyjmuje siΩ, i┐ bariera obrony zostaje prze│amana w≤wczas, gdy liczba tych kom≤rek w mililitrze zmniejszy siΩ poni┐ej 200 (u os≤b zdrowych wynosi oko│o 1000). W≤wczas nastΩpuje gwa│towna replikacja wirusa i w ko±cu ca│kowite za│amanie odporno£ciowe. W odpowiedzi przeciwwirusowej najwiΩksze znaczenie maj╣ cytotoksyczne kom≤rki CD8. Stwierdzono zdolno£µ rozpoznawania przez nie specyficznych epitop≤w w obrΩbie glikoprotein otoczki, bia│ka kodowanego przez gen gag, oraz innych produkt≤w, w tym tak┐e odwrotnej transkryptazy. Ten rodzaj kom≤rek cytotoksycznych pojawia siΩ wcze£nie po zaka┐eniu. Maj╣ one w│a£ciwo£ci zabijania zaka┐onych kom≤rek zanim te rozpoczn╣ replikowaµ cz╣stki wirusowe, co powoduje zmniejszenie liczby cz╣stek HIV. Aktywno£µ kom≤rek cytotoksycznych prawdopodobnie umo┐liwia wieloletni okres trwania nosicielstwa bezobjawowego. Szczeg≤lnie interesuj╣cym modelem bada± s╣ osoby, u kt≤rych nie dochodzi do progresji infekcji, mimo jej d│ugoletniego trwania (patrz ni┐ej). Chocia┐ jest tu wiele niejasno£ci, zwr≤cono uwagΩ, i┐ u tych os≤b wystΩpuj╣ limfocyty CD8+ ograniczaj╣ce mo┐liwo£µ przenoszenia zaka┐enia z limfocyt≤w CD4 na mononukleary krwi obwodowej. 0 ile hodowla czystych limfocyt≤w CD4 HIV+, pochodz╣cych od os≤b zaka┐onych przez wiele lat i nie rozwijaj╣cych AIDS, │atwo zaka┐a mononukleary aktywowane fitohemaglutynin╣, o tyle dodanie CD8 pochodz╣cych od tego samego dawcy co limfocyty CD4, blokuje in vitro takie zaka┐enie. Poniewa┐ taki sam efekt wywiera supernatant z hodowli ww. limfocyt≤w CD8, ich oddzia│ywanie odbywa siΩ najprawdopodobniej poprzez wytwarzanie do tej pory nieznanej cytokiny o nazwie czynnik przeciwwirusowy. Hamuje ona transkrypcjΩ HIV. Znane s╣ przypadki nadwra┐liwo£ci limfocyt≤w CD8 na antygeny HIV u os≤b bez cech zaka┐enia, kt≤re mia│y kontakty seksualne z nosicielami HIV. Opisano tak┐e przypadki cytotoksyczno£ci skierowanej przeciwko antygenom HIV (zale┐nej od MHC klasy I) u pracownik≤w s│u┐by zdrowia. Ulegli oni ekspozycji na wirusa, lecz nie dokonali serokonwersji w anty-HIV. Byµ mo┐e jest to zwi╣zane z ma│╣ liczb╣ zaka┐aj╣cych cz╣stek HIV, jednak┐e wystarczaj╣cych do rozwiniΩcia odporno£ci kom≤rkowej. Ostatnio opisano przypadek dziecka, u kt≤rego wyhodowano z mononuklear≤w krwi obwodowej HIV-1 w 19. i 51. dniu ┐ycia z negatywizacj╣ odczyn≤w serologicznych i wielokrotnymi ujemnymi wynikami hodowli oraz bada± metod╣ PCR na obecno£µ kwas≤w nukleinowych HIV (obserwacje do 5 roku ┐ycia). Aktywno£µ limfocyt≤w CD8 wystΩpuje tak┐e w wΩz│ach ch│onnych. Wp│ywa ona w okresie zaka┐enia bezobjawowego na hamowanie replikacji wirusa. Nie jest jasne, dlaczego w miarΩ trwania zaka┐enia aktywno£µ limfocyt≤w CD8 zmniejsza siΩ. Byµ mo┐e jest to zwi╣zane ze zjawiskiem apoptosis. Z drugiej strony, ten sam mechanizm mo┐e doprowadziµ do niszczenia kom≤rek CD4-TH1, co wy│╣cza dzia│anie cytokin nasilaj╣cych odpowiedƒ kom≤rkow╣. / Poradnik dla stomatolog≤w /
| |  |
Ostatnio wyodrΩbniono grupΩ os≤b (oko│o 7%), kt≤re pomimo zaka┐enia trwaj╣cego przesz│o 12 lat (nawet do 15) nie wykazuj╣ progresji choroby. Okre£lono ich charakterystyczne cechy. S╣ to: bardzo ma│a wiremia, zaka┐enie szczepem o mniejszych w│a£ciwo£ciach cytopatycznych, nie wystΩpowanie anty-HIV nasilaj╣cych zakaƒno£µ. Poza tym - aktywno£µ kom≤rek Th1 jest wiΩksza ni┐ Th2, a kom≤rki CD8 wykazuj╣ du┐╣ aktywno£µ przeciwwirusow╣. Struktura wΩz│≤w ch│onnych jest zachowana. Hodowla HIV z krwi daje najczΩ£ciej wyniki ujemne, lecz niekiedy udaje siΩ tego dokonaµ. Metod╣ PCR w omawianej tu grupie stwierdzono, w por≤wnaniu z zaka┐onymi wykazuj╣cymi cechy postΩpu choroby, niski stopie± wiremii oraz wirusowego DNA i RNA. W pojedynczych przypadkach wykazano, ┐e HIV u zaka┐onych bez postΩpu choroby ma zmiany typu delecji w genie nef. Czy szczeg≤lne rodzaje mutant≤w HIV s╣ przyczyn╣ opisywanych tu zjawisk - pozostaje spraw╣ otwart╣. Osoby te stanowi╣ prawdopodobnie grupΩ heterogenn╣. U niekt≤rych z nich byµ mo┐e do ko±ca ┐ycia nie rozwinie siΩ choroba, a u innych bΩdzie dochodzi│o do powolnej dysfunkcji odporno£ci. / Poradnik dla stomatolog≤w /
| |  |
Patogeneza zmian w o£rodkowym uk│adzie nerwowym jest bardzo z│o┐ona. Po£rednio lub bezpo£rednio - HIV wywo│uje rozleg│e spustoszenia zar≤wno w m≤zgu, jak i w rdzeniu krΩgowym oraz zaburzenia czynno£ciowe na obwodzie. Rozwija siΩ demencja zwi╣zana z AIDS (ADC: AIDS dementia complex). Na podstawie bada± neuropatologicznych g│≤wne zmiany w ADC to: - zanik kory m≤zgowej (niedob≤r wagi m≤zgu u dzieci);
- rozsiana astrogliosis;
- pobudzenie mikrogleju;
- utrata neuron≤w i (lub) uszkodzenia dendryt≤w w neocortex.
Zmiany w m≤zgowiu wystΩpuj╣ ju┐ w okresie nosicielstwa bezobjawowego (badania przeprowadzono u os≤b HIV+, kt≤re zginΩ│y w wyniku wypadk≤w). Wczesny zanik kory, zapalenie naczy±, degeneracja mieliny i astrocytoza - to najczΩstsze znaleziska.HIV wnika do m≤zgu poprzez kom≤rki £rodb│onka splot≤w naczyniowych lub przej£cie zaka┐onych limfocyt≤w i monocyt≤w przez uszkodzon╣ barierΩ krew - p│yn m≤zgowo-rdzeniowy. Bardzo istotne znaczenie maj╣ receptory kom≤rkowe HIV. Wirus mo┐e wnikn╣µ do kom≤rek nie maj╣cych cz╣steczki CD4. Uwa┐a siΩ, ┐e funkcje takie mog╣ pe│niµ tak┐e: receptor Fc, glikolipidy (jak galC) i LFA-1 (jest to jedna z integryn wystΩpuj╣ca na limfocytach B i T, monocytach i granulocytach). Jednak┐e efektywno£µ zaka┐enia kom≤rek bez receptora CD4 jest wielokrotnie mniejsza ani┐eli tych, kt≤re s╣ wyposa┐one w t╣ cz╣steczkΩ. I tak, kom≤rki z receptorem Fc ulegaj╣ zaka┐eniu 20 tys. razy mniej efektywnie. Cz╣stka galC wi╣┐e siΩ r≤wnie dobrze z gp120 jak z CD4. Jednak efektywno£µ zaka┐enia kom≤rek wykazuj╣cych ekspresjΩ galC jest 1000 razy mniejsza ani┐eli kom≤rek CD4+. Zaka┐eniu ulegaj╣ przede wszystkim kom≤rki z linii makrofagowej (makrofagi spoczynkowe, oko│onaczyniowe, mikroglej). Jednak┐e ostatnio przedstawiono dowody na mo┐liwo£µ infekcji HIV takich kom≤rek makrogleju, jak astrocyty i oligodendrocyty, a nawet neurony. Uszkadzaj╣ce oddzia│ywanie na m≤zg jest prawdopodobnie zwi╣zane z produktami pobudzonych kom≤rek zar≤wno makrofag≤w (mikroglej), jak i reaktywnych astrocyt≤w. S╣ to: cz╣stki adhezji miΩdzykom≤rkowej (np. ICAM-l, intracellular adhesion molecule, jeden z tzw. receptor≤w zasiedlania limfocyt≤w), cytokiny/czynniki wzrostu (interleukina-1 i 6, GM-CSF: granulocyte-macrophage colony stimulating factor, czynnik stymuluj╣cy tworzenie kolonii granulocyt≤w i makrofag≤w; TNF: tumor necrosis factor, czynnik martwicy nowotworu) i inne. / Poradnik dla stomatolog≤w /
| |  |
Przeniesienie zaka┐enia z ciΩ┐arnej matki na dziecko ma liczne uwarunkowania. Ryzyko to jest oceniane na 15-35% (mniejsze w Europie ani┐eli w Afryce). Czynnikiem wysoce sprzyjaj╣cym jest poziom obci╣┐enia wirusem organizmu matki. Inne, to niskie warto£ci limfocyt≤w CD4 i zaawansowane zaka┐enie. Kontrowersyjnie przedstawia siΩ problem zwi╣zku z ryzykiem zaka┐enia - wystΩpowanie wariant≤w typu SI. Czynniki, takie jak zaka┐enia drobnoustrojami przenoszonymi drog╣ p│ciow╣ i chorioamnionitis, powoduj╣ce uszkodzenie bariery │o┐yskowej, mog╣ zwiΩkszaµ liczbΩ cz╣stek wirusa w kanale rodnym. Wysokie miana przeciwcia│ neutralizuj╣cych, a zw│aszcza ich du┐e powinowactwo do szerokiego spektrum epitop≤w HIV, dzia│aj╣ jako czynniki ochronne. Wczesne wykrywanie zaka┐e± p│odu jest mo┐liwe poprzez hodowlΩ wirusa, wykrycie jego materia│u genetycznego metod╣ PCR albo stwierdzenie antygenemii. Przeciwcia│a anty-HIV mog╣ utrzymywaµ siΩ (przeniesienie bierne przez │o┐ysko) do 18 miesiΩcy. Dlatego dopiero po tym terminie ich stwierdzenie jest dowodem zaka┐enia (aktywna synteza anty-HIV przez ustr≤j dziecka). Czu│o£µ hodowli HIV oraz metody PCR wynosi oko│o 40% w dniu urodzenia, lecz po miesi╣cu siΩga 90%. Do zaka┐enia dochodzi najczΩ£ciej w czasie porodu, a bardzo rzadko wewn╣trzmacicznie. Objawy zaka┐enia HIV u dziecka wystΩpuj╣ najczΩ£ciej po kilku miesi╣cach lub latach. Szybki rozw≤j choroby jest czΩstszy, ani┐eli u doros│ych. Jest to zwi╣zane z niepe│n╣ dojrza│o£ci╣ uk│adu odporno£ciowego w okresie zaka┐enia. Kom≤rki T noworodka maj╣ ograniczon╣ biologicznie zdolno£µ do wytwarzania cytokin, takich jak interleukiny 3 i 4, czy interferon-y. Powoduje to niedostateczny rozw≤j odpowiedzi humoralnej i kom≤rkowej. Zaka┐enie HIV i rozw≤j AIDS jest jednym z najbardziej z│o┐onych zjawisk spo£r≤d wszystkich chor≤b zakaƒnych znanych w patologii cz│owieka. / Poradnik dla stomatolog≤w /
| |  | ⌐ 1998 SONAR | |
|
|