|
V²skyt
Vodφk je nejrozÜφ°en∞jÜφ prvek v celΘm vesmφru a t°etφ nejrozÜφ°en∞jÜφ prvek na Zemi. Vyskytuje se voln∞ i vßzan² ve slouΦeninßch. Voln² vodφk se nalΘzß se nap°. v plynnΘm obalu hv∞zd. Na Zemi se voln² vodφk za b∞₧n²ch podmφnek nevyskytuje, a proto je zde vßzßn jenom ve slouΦeninßch. Nejv∞tÜφ mno₧stvφ vodφku je vßzßno ve vod∞, kterß pokr²vß v∞tÜinu zemskΘho povrchu, ale je vßzßn i v r∙zn²ch organick²ch i anorganick²ch slouΦeninßch. Je to takΘ v²znamn² biogennφ prvek.
V p°φrod∞ se vyskytuje jako sm∞s t°φ izotop∙:
Vlastnosti
Je to bezbarv² plyn bez chuti a zßpachu, kter² je lehΦφ ne₧ vzduch. Molekulov² vodφk je pom∞rn∞ stabilnφ a dφky vysokΘ hodnot∞ vazebnΘ energie takΘ mßlo reaktivnφ. S v∞tÜinou prvk∙ se proto sluΦuje a₧ za zv²ÜenΘ teploty nebo za p°φtomnosti katalyzßtor∙:
H2 + Cl2 -> 2HCl
N2 + 3H2 -> 2NH3
H2 + S -> H2S
2H2 + O2 -> 2H2O + uvoln∞nφ energie
Reakce vodφku b²vajφ provßzeny uvol≥ovßnφm tepla (exotermnφ reakce) a n∞kdy takΘ sv∞teln²m efektem - ho°enφm. V²znamnΘ jsou redukΦnφ vlastnosti vodφku, kterΘ se vyu₧φvajφ k v²rob∞ n∞kter²ch kov∙ z jejich oxid∙:
CuO + H2 -> Cu + H2O
WO3 + 3H2 -> W + 3H2O
Naproti tomu atomov² vodφk (tzv. vodφk ve stavu zrodu) je velmi reaktivnφ a reaguje s celou °adou lßtek ji₧ za nφzk²ch teplot. Je to takΘ jako molekulov² vodφk silnΘ redukΦnφ Φinidlo, ale existuje velmi krßtkou dobu a sluΦuje se na vodφk molekulov².
Jinak je to typick² nekov, kter² tvo°φ vodφkovΘ m∙stky s dusφkem, kyslφkem a fluorem. Vodφk byl objeven roku 1766 anglick²m chemikem a fyzikem Henry Cavendishem (1731-1810).
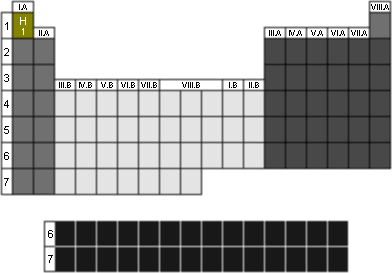
Umφst∞nφ prvku v periodickΘ tabulce
Laboratornφ p°φprava
V laborato°i se m∙₧e vodφk p°ipravovat reakcφ neuÜlechtil²ch kov∙ s kyselinami nebo hydroxidy v tzv. Kippov∞ p°φstroji:
Zn + 2HCl -> ZnCl2 + H2
Zn + 2NaOH + 2H2O -> Na2[Zn(OH)4] + H2
Dßle m∙₧eme vodφk zφskat elektrol²zou vody, kterß obsahuje malΘ mno₧stvφ H2SO4 nebo NaOH pro zv²Üenφ vodivosti. Elektrol²za se provßdφ v Hoffmanov∞ p°φstroji, kde se vodφk vyluΦuje na katod∞:
2H3O+ + 2e- -> 2H2O + H2
DalÜφ v²robnφ metodou je reakce s1 a s2 prvk∙ s vodou:
2Na + 2H2O -> 2NaOH + H2
Poslednφm v²znamn∞jÜφm postupem je reakce vodnφ pßry se ₧elezem:
3Fe + 4H2O -> Fe3O4 + 4H2
Pr∙myslovß v²roba
Pr∙myslov∞ se m∙₧e vodφk stejn∞ jako v laborato°i vyrßb∞t n∞kolika r∙zn²mi metodami. Prvnφ metodou je termick² rozklad methanu za velmi vysokΘ teploty (1200░C):
CH4 -> C + 2H2
Reakcφ vodnφho plynu s vodnφ pßrou za p°φtomnosti katalyzßtor∙ a p°i teplot∞ 300░C m∙₧eme zφskat velmi Φist² vodφk, kter² se pou₧φvß nap°. ke ztu₧ovßnφ tuk∙:
CO + H2 + H2O(g) -> CO2 + 2H2
DalÜφm v²robnφm postupem je reakce vodnφ pßry s roz₧haven²m koksem za teploty 1000░C:
C(s) + H2O(g) -> CO(g) + H2(g)
Vodφk vznikß takΘ jako vedlejÜφ produkt p°i v²rob∞ hydroxidu sodnΘho (NaOH) - elektrol²za vodnΘho roztoku NaCl:
2NaHgn + 2H2O -> 2NaOH + H2 + 2nHg
Pou₧itφ
Vodφk mß °adu v²znamn²ch pou₧itφ mezi n∞₧ pat°φ nap°φklad v²roba r∙zn²ch chemick²ch slouΦenin (amoniak - NH3, kyselina dusiΦnß - HNO3, methylalkohol - CH3OH, r∙znß dusφkatß hnojiva, atd.), v²roba n∞kter²ch kov∙ (redukcφ z jejich oxid∙) nebo ztu₧ovßnφ tuk∙. D°φve se pou₧φval takΘ ke sva°ovßnφ a °ezßnφ kov∙ (kyslφkovodφkov² plamen. Kapaln² vodφk se pou₧φvß jako raketovΘ palivo, ale m∙₧e b²t zdrojem energie i pro jinß za°φzenφ. Vodφk se p°epravuje a uchovßvß v ocelov²ch lahvφch oznaΦen²ch Φerven²m pruhem.
SlouΦeniny
H2O - voda
nejb∞₧n∞jÜφ a nejrozÜφ°en∞jÜφ chemickß slouΦenina
hydridy - binßrnφ (dvouprvkovΘ) slouΦeniny vodφku
podrobn∞jÜφ informace o konkrΘtnφch hydridech naleznete na jednotliv²ch strßnkßch o chemick²ch prvcφch